Matīss Linde, Kristīne Jubele: COVID un aritmijas
2019. gada koronavīrusa (CoV-19) infekcijas slimība sākotnēji izcēlās Ķīnas pilsētā Uhaņā. Pirmo oficiālo saslimšanas gadījumu Latvijā fiksēja 2020. gada 2. martā un 2020. gada 11. martā Pasaules Veselības organizācijas pārstāvji publiski izsludināja pandēmijas sākumu. Aptuveni divu gadu laikā kopš pandēmijas sākuma iegūti relatīvi plaši dati par slimības izplatību, patofizioloģiju, profilaksi, terapiju, kā arī ietekmi tieši uz sirds un asinsvadu sistēmu. Vairākos pētījumos apliecināts, ka sirds un asinsvadu sistēmas saslimšanas ir saistītas ar smagāku klīnisko gaitu un augstāku mirstību pacientiem ar CoV-19. Veicot pētījumu analīzi par CoV-19 nelabvēlīgiem prognozes rādītājiem, pierādīts, ka sirds un asinsvadu sistēmas saslimšanas trīskāršo risku smagai CoV-19 slimības klīniskajai gaitai (tas ir, letālu iznākumu, hospitalizāciju intensīvās terapijas nodaļā, mākslīgās plaušu ventilācijas pielietošanu vai slimības progresiju).
CoV-19 ir viena pavediena ribonukleīnskābes (RNS) vīruss, uz kā virsmas projicējas pīķa proteīni un, salīdzinoši ar citiem vīrusa veidiem, CoV-19 izceļas tieši ar augstu dzīvotspēju un paaugstinātu infekciozitāti. CoV-19 iekļūst šūnā ar pīķa proteīniem caur angiotenzīna konvertējošā enzīma 2 (ACE-2) receptoru un transmembranālu proteīnu. ACE-2 ir daudzfunkcionāls proteīns, kura primārā fizioloģiskā loma ir enzimātiska pāreja no angiotenzīna II uz angiotenzīnu (1-7) un angiotenzīna I pāreja uz angiotenzīnu (1-9), kas ir protektīvi kardiovaskulāri peptīdi. Visaugstākā ACE-2 izpausme ir tieši plaušu alveolu sīko asinsvadu šūnās. Iekļūstot ACE-2 receptoru saturošās šūnās, vīruss vairojas, veidojot jaunus vīrusa pavedienus, kas tiek apstrādāti viriona saturošā vezikulā un, saplūstot ar šūnas membrānu, ārpus šūnas izdala jaunas vīrusa kopijas. Neskaitot plaušas, papildus ACE-2 receptori ļoti aktīvi ir sirds muskuļu šūnās, asinsvados un kuņģa zarnu traktā. Papildus jānorāda, ka būtiska loma ir CD209 receptoram, ko ekspresē uz makrofāgiem, kas ir imūnās sistēmas šūna. Viena no tā galvenajām funkcijām ir ķermenim svešu daļiņu iznīcināšana, tomēr CoV-19 caur šo receptoru var iekļūt makrofāgos un šīs šūnas lokalizējas sirds un asinsvadu audos. Svarīgi piebilst, ka smagas CoV-19 norises gadījumā var veidoties pastiprināta imūnās sistēmas atbildes reakcija un no tās izrietoša iekaisuma citokīnu vētra. Iekaisuma citokīni ir imūnās sistēmas marķieri. Pieaugot šo marķieru koncentrācijai - kā galvenos norādot interleikīnu-1 (IL-1), interleikīnu-6 (IL-6) un tumora nekrozes faktoru alfa (TNF-alfa), veidojas dažādu audu bojājums, tajā skaitā sirds audu.
Tieši iepriekš minētie iekaisuma citokīni ir saistīti ar efektiem, kas var provocēt aritmijas. Dažādu tiešu un netiešu kardiālu ietekmes mehānismu rezultātā pārlieku stipras imūnās sistēmas reakcijas dēļ veidojas sirds strukturālas un elektriskas izmaiņas. Jāpiebilst, ka pandēmijas sākumā CoV-19 infekciju un sirds aritmijas asociēja ar specifisku infekcijas slimības mehānismu, kā, piemēram, sirds bojājumu tiešas vīrusu invāzijas dēļ vai aritmijas provocējošiem efektiem no dažādiem medikamentiem (piemēram, hlorokvīnu, azitromicīnu, proteāzes inhibitoriem un citiem). Tomēr kļuva skaidrs, ka tiešs vīrusa inducēts sirds bojājums ir mazākajai pacientu daļai, kam veidojās vai paasinājās aritmijas. Jāteic gan, ka iepriekš minētie un citi medikamenti ir saistīti ar paaugstinātu aritmijas risku. Svarīgi fiksēt blakus efektus no medikamentiem, kas var tikt pielietoti kā antivīrusu līdzekļi, tomēr veicināt QT intervāla pagarināšanos elektrokardiogrammā, izraisīt polimorfu kambaru tahikardiju un pat kambaru fibrilācijai, kas ir dzīvībai bīstamas aritmijas. Citohroma P450 sistēma oksidācijas procesā metabolizē medikamentus un citas ķīmiskas vielas, lai tās varētu izvadīt no organisma, bet, nomācot šo sistēmu, medikamentu darbība kļūst ilgāka, kas arī veicina kambaru repolarizācijas pagarināšanos un predisponē iepriekš minētajām sirds aritmijām. Līdz šim noskaidrots, ka smagāka CoV-19 klīniskā gaita ir pacientam ar vairākām blakus saslimšanām, kurš lieto arī citus medikamentus. Attiecīgi, inhibējot citohroma P450 sistēmu, organisms nespēj metabolizēt tādu medikamentu grupas kā antipsihotiskos līdzekļus, antidepresantus, antihistamīnus, makrolīdus, fluorokvinolonus un citu grupu preperātus, tādējādi vēl vairāk paaugstinot risku attīstīties sirds aritmijām. Pierādījumi liecina, ka IL-6 arī tieši inhibē hERG kālija kanālu un inhibē citohroma P450 sistēmu, attiecīgi, pagarinoties QT intervālam. Papildus IL-6, TNF alfa un IL-1 var pagarināt kambaru darbības potenciāla ilgumu, izmainot sirds muskuļu šūnu jonu kanālu ekspresiju un funkciju, tādējādi paaugstinot risku attīstīties sirds aritmijām [8].
Papildus kā potenciālus aritmiju provocējošus faktorus saistībā ar CoV-19 infekciju var minēt audu hipoksiju, kas veidojas no plaušu bojājuma. Gan pastiprināta imūnās sistēmas reakcija, gan audu hipoksija ir saistīta ar sirds bojājumu, ko apliecina paaugstināts Troponīna I (sirds nekrozes marķiera) līmenis. Papildus zināms, ka paaugstināts iekaisuma citokīnu skaits tieši saistīts ar Troponīna I koncentrācijas pieaugumu. Kļuvis skaidrs, ka atsevišķiem pacientiem ar CoV-19 infekciju vai citu izsaucēju ierosinātām pneimonijām var attīstīties dzīvībai bīstamas aritmijas, neraugoties uz to, ka nav smagas elpošanas sistēmas mazspējas, bet ir izteiktas imūnās sistēmas reakcijas izraisīts sirds bojājums. Ir zinātniski ziņojumi, kas apstiprina prognozējamu riska pieaugumu attīstīties priekškambaru un kambaru aritmijām CoV-19 hospitalizētiem pacientiem ar paaugstinātu IL-6 un IL-10 līmeni.
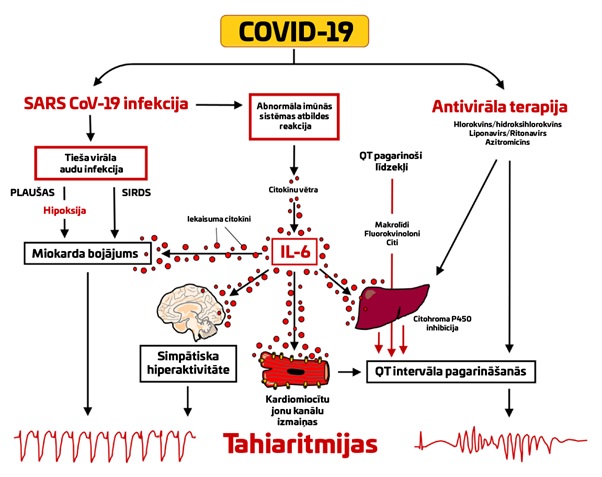
Iespējamie mehānismi kambaru aritmijas attīstības riskam pacientiem ar CoV-19. Adaptēts no Lazzerini PE, Boutjdir M, Capecchi PL. COVID-19, Arrhythmic Risk, and Inflammation: Mind the Gap! Circulation. 2020 Jul 7;142(1):7-9.
2021.gadā Amerikas Savienotajās Valstīs veikts pētījums, apkopojot to pacientu datus, kuriem ir implantētas sirds ritmu monitorējošas ierīces, kas fiksēja ātriju fibrilācijas epizodes biežumu un ilgumu. Ātriju fibrilācija ir biežākā aritmija, kuras laikā sirds priekškambaros ir pilnīgs elektrisks haoss, tāpēc priekškambaru saraušanās nenotiek, kas savukārt var izraisīt asins recekļu veidošanos sirdī. Šajā pētījumā analizēts laika periods 100 dienu garumā no pandēmijas sākuma, salīdzinot ar identisku laika periodu pirms gada. Ātriju fibrilācijas epizodes CoV-19 pandēmijas laikā fiksēja vairāk. Epizodes, kas pārsniedza sešas minūtes, piefiksētas par 33% vairāk, epizodes, kas pārsniedza stundu, piefiksētas par 65% vairāk un epizodes, kas pārsniedza sešas stundas, piefiksētas par 54% vairāk. Tomēr ne visi pacienti pārslimoja CoV-19 un ne visi pārslimoja ar smagu klīnisko gaitu. Tas ļauj identificēt citus riska faktorus, ko iespējams saistīt ar paaugstinātu sirds aritmiju risku. Līdz ar ko arī šī pētījuma ietvaros tiek izvirzīta hipotēze, ka paaugstināts ātriju fibrilāciju epizožu biežums un ilgums ir saistīts ar dzīves stila izmaiņām, pielāgojoties jaunam dzīves režīmam un ierobežojumiem. Kā nozīmīgus faktorus var minēt - sociālo distancēšanos, darbu no mājām vai tā zaudēšanu, individuālus ekonomiskos faktorus, kas var izraisīt hronisku stresu, izmaiņas diētā, fizisko aktivitāšu samazināšanos, svara pieaugumu, pastiprinātu alkohola lietošanu, palielinot risku ātriju fibrilācijas attīstībai. Kā iepriekš minēts, āriju fibrilācija ir biežākā aritmija, kas saistīta ar Covid 19 infekciju. Akūtajā infekcijas periodā var pieņemt lēmumu aritmiju nepārtraukt, taču pēc atveseļošanās no Covid-19 noteikti jāvēršas pie kardiologa, lai lemtu par tālāko taktiku. Jāatceras arī, ka ātriju fibrilācija palielina sirds trombu veidošanās risku, kas var izraisīt insultu, tāpēc būtu jālieto antikogulanti (medikamentu grupa, kas šķidrina asinis un pie kuriem nepieder Aspirīns).
Klīnisko gadījumu sēriju pētījumā ir aprakstītas arī augstas pakāpes atrioventrikulāras (AV) blokādes četriem CoV-19 pacientiem (trīs pacienti vecumā virs 60 gadiem, viens - 42 gadus vecs), kuriem anamnēzē nav bijušas sirds aritmijas. AV blokāde ir situācija, kad impulss, kas rodas sirds priekškambaros, nenonāk kambaros. Lielākoties šāda situācija izraisa lēnu pulsu. Vienīgā kopīgā blakus slimība visiem pacientiem bija arteriāla hipertensija, kā arī virssvars un bija nepieciešama papildus skābekļa terapija. Jāpiebilst, ka visiem pacientiem AV blokādes izzuda spontāni, bet pacientam ar vairākām blakus saslimšanām bija nepieciešama īslaicīga sirds stimulācija. Iespējamie mehānismi, kas veidotu AV blokādi, norādīti jau iepriekš, tomēr vēl min saistību ar akūtu nieru mazspēju, kā rezultātā veidojas elektrolītu līdzsvara traucējumi un paaugstināts kālija līmenis asinīs. Tas veicina AV blokādi, tomēr nevienam no pētījumā iekļautajiem pacientiem nebija akūtas nieru mazspējas.
Pensilvānijas universitātes slimnīcas pētījumā deviņu nedēļu garumā iekļāva 700 pacientus, kurus hospitalizēja ar CoV-19. Kopā identificēja 53 sirds aritmijas notikumus - 25 pacientiem fiksēja ātriju fibrilāciju, deviņiem - klīniski nozīmīgu bradiaritmiju, 10 - nenoturīgu kambaru tahikardiju un deviņiem pacientiem sirds apstāšanos. Tā fiksēta tikai pacientiem, kurus hospitalizēja intensīvās terapijas nodaļā un kuriem bija vairākas blakus slimības - arteriāla hipertensija, cukura diabēts, obstruktīva miega apnoja, hroniska obstruktīva plaušu slimība, aknu slimības un hroniska nieru slimība. Galvenā atziņa no šī pētījuma, ka ar smagāku klīnisko ainu attiecīgi palielinās sirds aritmiju risks, it īpaši dzīvībai bīstamu aritmiju risks.
Vakcinācija pret CoV-19 infekcijas slimību novērš smagas norises saslimšanu ar CoV-19, tomēr gluži kā ar jebkuru citu līdzekli, arī no vakcinācijas var veidoties blakusefekti. Visplašāk min tieši miokardītu (sirds muskuļa iekaisums), ko nenoliedzami arī var saistīt ar sirds aritmiju paaugstinātu risku. Izraēlā starp divarpus miljoniem par 16 gadiem vecāku cilvēku, kas saņēma Pfizer-BioNTech vakcīnu, fiksēti 54 miokardīta gadījumi. Miokardīta prognozējamais biežums ir 2,13 gadījumi starp 100 000 vakcinēto. 22% no miokardīta gadījumiem definēti ar vidējas slimības norisi, pārējie - ar vieglu.
Šobrīd ir lielāka skaidrība par sirds aritmiju risku veicinošiem faktoriem un sastopamību, to iespējamiem cēloņiem un citu valstu novērojumiem. Lai labāk varētu sniegt atbalstu CoV-19 pacientiem, kuriem arī ir sirds un asinsvadu sistēmas saslimšanas, Eiropas kardiologu biedrības speciālisti izstrādājuši vadlīnijas, lai akcentētu svarīgāko informāciju, kas jāzina pacientam. Vadlīnijās akcentēti atsevišķi stāvokļi un saslimšanas, ko saista ar smagu CoV-19 norisi un tie ir šādi: vecums virs 65 gadiem un vismaz viena blakus saslimšana; par 70 gadiem vecāki pacienti; hroniska obstruktīva plaušu slimība; astma; hroniska sirds mazspēja; atsevišķas sirds aritmijas; koronāra artēriju slimība; pēdējos trīs mēnešos veikta koronārās artērijas revaskularizācija; ķermeņa masas indekss virs 35 kg/m2 vai virs 30 kg/m2 ar vismaz vienu vai vairākām blakus saslimšanām; sirpjveida anēmija; pēdējos sešos mēnešos veikta orgāna transplantācija; hipertrofiska kardiomiopātija ar obstrukciju; hroniska nieru slimība (glomerulārās filtrācijas ātrums zem 15 mL/min) un nekontrolēta cukura diabēta saslimšana. Ļoti svarīgi turpināt ārsta nozīmēto terapiju. Piemēram, raksta sākumā norādīta angiotenzīna konvertējošā enzīma divu receptora loma CoV-19 patoģenēzē. Lieto arī medikamentus, kas bloķē šo receptoru, lai ārstētu arteriālu hipertensiju, tomēr šo medikamentu lietošana neietekmē CoV-19 vīrusa iekļūšanu šūnās. Atsevišķos gadījumos būtu nepieciešama terapijas pielāgošana, īpaši, ja pacientu ar CoV-19 hospitalizē. Piemēram, CoV-19 terapijā var nozīmēt deksametazonu vai metilprednizolonu, kas var mijiedarboties ar varfarīnu, ko nereti pacienti lieto saistībā ar ātriju fibrilāciju trombozes veidošanās prevencijai, jo mijiedarbība var izpausties ar pastiprinātu varfarīna darbību un tādējādi ir nepieciešams monitorēt INR. Lietojot antiretrovirālus līdzekļus, piemēram, - remdesiviru, ir potenciāla iespēja mijiedarboties ar antiaritmiskiem līdzekļiem un būtu nepieciešams elektrokardiogrāfijas monitorings. Iesaka arī izvairīties no apiksabāna un rivaroksabāna lietošanas, kas ir antiokoagulācijas līdzekļi, ko arī var lietot ātriju fibrilācijas trombozes profilaksei. Iespējama mijedarbība arī ir statīna līdzekļiem - rosuvastatīnam vai atorvastatīnam un visbeidzot, antiretrovirālie līdzekļi var mijiedarboties ar varfarīnu un būtu nepieciešams monitorēt INR. Arī kolhicīnu var izmantot CoV-19 pacientu ārstēšanā un ir iespējama mijiedarbība ar statīniem, attiecīgi statīnu devas jāsamazina. Iespējama arī mijiedarbība ar CYP3A4 inhibitoriem (piemēram, tikagrelors) un attiecīgi būtu jāapsver kolhicīna devas samazināšana. Arī iepriekš pieminēto līdzekļu hlorokvīna un hidroksihlorokvīna preperāti var mijiedarboties ar beta blokatoriem un citiem QT pagarinošiem līdzekļiem, līdz ar ko būtu nepieciešams elektrokardiogrāfijas monitorings. Būtiski piebilst, ka iepriekš minētos līdzekļus CoV-19 infekcijas slimības ārstēšanā lielākoties pielieto tikai hospitalizētiem pacientiem un ārsta atbildība ir rēķināties ar potenciālu mijiedarbību ar citiem lietotiem medikamentiem.
Attiecībā uz CoV-19 vakcināciju, norādīts, ka vakcinācija ir un paliek efektīvs terapijas veids, kā novērst smagu CoV-19 infekcijas saslimšanu. Vakcinācijai ir maz kontrindikāciju un kardiovaskulāras saslimšanas nav to skaitā.
Visbeidzot, lai novērstu risku saslimt ar CoV-19, kas var palielināt risku sirds aritmiju attīstībai, nepieciešams ievērot profilaktiskus un preventīvus pasākumus: izvairīties no kontakta ar inficētiem cilvēkiem; ievērot divu metru distanci; mazgāt rokas ar ziepēm un siltu ūdeni vismaz 20 sekundes; klepojot vai šķaudot aizsegt muti vai degunu ar salveti vai elkoni; izvairīties pieskarties acīm, degunam un mutei, kontaktējoties ar citiem cilvēkiem; ievērot sanitārus apstākļus un lietot dezinfektorus virsmu tīrīšanai; ja ir drudža simptomi, klepus vai pneimonija, ievērot pašizolāciju un vērsties pēc medicīniskas palīdzības, kā arī neaizmirst par fiziskām aktivitātēm, kas ir būtiski arī venozas trombembolijas prevencijai un vispārējas dzīves kvalitātes veicināšanai.
Izmantotā literatūra
1) https://www.spkc.gov.lv/lv/aktualitates-par-covid-19
3) The Task Force for the management of COVID-19 of the European Society of Cardiology, European Society of Cardiology guidance for the diagnosis and management of cardiovascular disease during the COVID-19 pandemic: part 1—epidemiology, pathophysiology, and diagnosis, European Heart Journal, Volume 43, Issue 11, 14 March 2022, Pages 1033–1058, https://doi.org/10.1093/eurheartj/ehab696
4) Figliozzi S, Masci PG, Ahmadi N et al. Predictors of adverse prognosis in COVID-19: a systematic review and meta-analysis. Eur J Clin Invest 2020;50:e13362.
5)Lazzerini, P.E., Laghi-Pasini, F., Boutjdir, M. et al. Inflammatory cytokines and cardiac arrhythmias: the lesson from COVID-19. Nat Rev Immunol 22, 270–272 (2022). https://doi.org/10.1038/s41577-022-00714-3 https://www.nature.com/articles/s41577-022-00714-3#citeas
6)Siddiq, M. M. et al. Functional effects of cardiomyocyte injury in COVID-19. J. Virol. 96, e0106321 (2022).
7)Guan, H. et al. Arrhythmias in patients with coronavirus disease 2019 (COVID-19) in Wuhan, China: incidences and implications. J. Electrocardiol. 65, 96–101 (2021).
8)Lazzerini PE, Boutjdir M, Capecchi PL. COVID-19, Arrhythmic Risk, and Inflammation: Mind the Gap! Circulation. 2020 Jul 7;142(1):7-9. doi: 10.1161/CIRCULATIONAHA.120.047293.
9)Catherine J O’Shea, Melissa E Middeldorp, Gijo Thomas, Curtis Harper, Adrian D Elliott, Noemi Ray, Kevin Campbell, Dennis H Lau, Prashanthan Sanders, Atrial fibrillation burden during the coronavirus disease 2019 pandemic, EP Europace, Volume 23, Issue 9, September 2021, Pages 1493–1501, https://doi.org/10.1093/europace/euab099
10) Dagher L, Wanna B, Mikdadi G, Young M, Sohns C, Marrouche NF. High-degree atrioventricular block in COVID-19 hospitalized patients. Europace. 2021 Mar 8;23(3):451-455. doi: 10.1093/europace/euaa333.
11)Bhatla A, Mayer MM, Adusumalli S, Hyman MC, Oh E, Tierney A, Moss J, Chahal AA, Anesi G, Denduluri S, Domenico CM, Arkles J, Abella BS, Bullinga JR, Callans DJ, Dixit S, Epstein AE, Frankel DS, Garcia FC, Kumareswaram R, Nazarian S, Riley MP, Santangeli P, Schaller RD, Supple GE, Lin D, Marchlinski F, Deo R. COVID-19 and cardiac arrhythmias. Heart Rhythm. 2020 Sep;17(9):1439-1444. doi: 10.1016/j.hrthm.2020.06.016.
12)Task Force for the management of COVID-19 of the European Society of Cardiology. ESC guidance for the diagnosis and management of cardiovascular disease during the COVID-19 pandemic: part 2-care pathways, treatment, and follow-up. Eur Heart J. 2022 Mar 14;43(11):1059-1103. doi: 10.1093/eurheartj/ehab697. Erratum in: Eur Heart J. 2021 Dec 20.
13)Witberg G, Barda N, Hoss S, Richter I, Wiessman M, Aviv Y, Grinberg T, Auster O, Dagan N, Balicer RD, Kornowski R. Myocarditis after Covid-19 Vaccination in a Large Health Care Organization. N Engl J Med. 2021 Dec 2;385(23):2132-2139. doi: 10.1056/NEJMoa2110737.
Foto: Shutterstock
Raksts publicēts „Ārsts.lv” 2022. gada augusta numurā!
Portālā "Ārsts.lv" publicēto rakstu pārpublicēšana iespējama tikai, saskaņojot ar portāla redakciju!



