Inga Narbute: Aortas vārstuļa stenozes invazīva ārstēšana
Vēsture
Veselības aprūpe pēdējos simts gados pieredzējusi milzīgi strauju diagnostisko un ārstniecisko metožu evolūciju. Hipokrāta laiks, kad vienīgie diagnostikas rīki bija pacienta novērošana, fizikāla izmeklēšana un loģiska domāšana, nav salīdzināms ar mūsdienām, kad izmantojam ļoti sarežģītas diagnostikas un ārstniecības metodes, tai skaitā robotu medicīnu.
Vēl 19. gadsimta beigās valdīja uzskats, ka sirds operācijas ir neētiskas, neprofesionālas un nepieļaujamas. Teodors Bilrots (1821–1894) sludināja, ka ķirurgs, kas mēģinās operēt sirdi, nav pelnījis kolēģu cieņu. Neskatoties uz to, 1896. gada 9. septembrī vācu ķirurgs Ludvigs Rēns (1849–1930) veica pirmo sekmīgo sirds operāciju – labā kambara durtas brūces revīziju, pēc kuras pacients izdzīvoja. Tādējādi 1896. gads, pēc vairāku vēsturnieku domām, uzskatāms par kardioķirurģijas dzimšanas gadu.
Aortas vārstuļa operāciju mēģinājumi aizsākti 20. gadsimta 40. gados. 1965. gadā izmantots jau pirmais bioloģiskais vārstulis. 2002. gada 16. aprīlī Alēns Kribjē veica pirmo transkatetrālo aortas vārstuļa implantāciju (TAVI) dzīvam cilvēkam: 57 gadus vecam smagas stenozes pacientam, kardiogēnā šokā multiplām blakusslimībām, kuru dēļ ķirurģiska ārstēšana nebija iespējama. Tas uzsāka jaunu šīs slimības ārstēšanas ēru un deva iespēju normāli dzīvot pacientiem, kuri līdz šim to nespēja.
Latvijā pirmā TAVI (ar transapikālu pieeju) tika veikta 2009. gada 30. septembrī profesoru Andreja Ērgļa un Pētera Stradiņa vadībā. Savukārt pirmā transfemorālā aortas vārstuļa bioprotēzes implantācija notika nedaudz vēlāk – 2010. gada 22. februārī – profesora Andreja Ērgļa vadībā, piedaloties dr. A. Rudzītim un dr. A. Dombrovskim.
Īsumā par aortas vārstuļa stenozi
Aortas vārstuļa stenozes jeb sašaurināšanās (AS) biežākais iemesls ir vecuma izraisītas deģeneratīvas vārstuļa viru izmaiņas. ASV un Eiropas valstīs cilvēkiem virs 65 gadu vecuma kalcificējošas stenozes biežums ir 2–7%, vecumā virs 75 gadiem – 5%. Tā ir biežākā iegūtā sirdskaite, kuras dēļ ir nepieciešama operācija – vārstuļa nomaiņa.
Uzlabojoties veselības aprūpei un tādējādi arī pacientu dzīvildzei, aortālās stenozes izplatībai ir tendence pieaugt.
Aortas vārstuļa stenoze ir slimība ar garu latento periodu un tam sekojošu strauju slimības un simptomu progresēšanu, kam ir augsts mirstības risks. Ja pacients netiek ārstēts, divu gadu laikā no simptomu parādīšanās brīža, šis risks sasniedz apmēram 50%, bet 5 gadu laikā – pat 80%. Smagas pakāpes gadījumā efektīvākais veids ir vārstuļa nomaiņa, jo simptomātiska ārstēšana ar medikamentiem nav guvusi labus rezultātus – viena gada dzīvildzi sasniedz 60%, bet piecu gadu – tikai 32% pacientu.
Ārstēšana
Lai samazinātu simptomus un uzlabotu dzīvildzi, ilgu laiku par smagas pakāpes ārstēšanas zelta standartu šai gadījumā uzskatīja ķirurģisku vārstuļa nomaiņu. Tomēr daļai pacientu tas nav iespējams vecuma, nopietnu blakusslimību, iepriekšēju operāciju vai citas terapijas dēļ, jo ir ļoti augsts mirstības risks. Pētījumu metaanalīzes dati rāda, ka līdz pat 30% simptomātisku pacientu ar aortas vārstuļa stenozi netiek sniegta ķirurģiska palīdzība komplikāciju riska dēļ.
Uz laiku mazināt simptomus un uzlabot vārstuļa funkciju šādā gadījumā var vārstuļa balonvalvuloplastija jeb paplašināšana ar balonu. Tomēr tās rezultāts nav pilnīgs un ilgnoturīgs, tāpēc metode vērtējama kā paliatīva procedūra vai tilts, lai stabilizētu hemodinamiski nestabilus pacientus pirms vārstuļa nomaiņas.
TAVI kā alternatīvu klasiskajai operācijai izmanto augsta vai atsevišķos gadījumos vidēja ķirurģiskā riska pacientiem, kā arī cilvēkiem, kam dažādu iemeslu dēļ konvencionālā operācija mākslīgās asinsrites apstākļos nav iespējama.
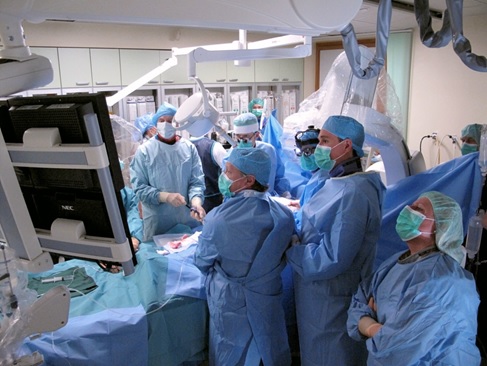
3. attēls. Pirmā TAVI operācija Latvijā. Foto no Latvijas Kardioloģijas centra arhīva
“Sirds komanda”
TAVI operācija ir tikai beigu posms, kuru veic kardioķirurgi vai invazīvie kardiologi, bet tai ir nepieciešama multidisciplināras komandas sadarbība, lai izvērtētu, kuru metodi izmantot konkrētajam pacientam, un viņu atbilstoši sagatavotu un vadītu. Tā saucamo “sirds komandu” veido klīniskais kardiologs, invazīvais kardiologs, kardioķirurgs, anesteziologs, radiologs un nepieciešamības gadījumā citi klīniskie speciālisti, kā arī medicīnas māsa.
Indikācijas vārstuļa nomaiņas stratēģijai (gan ķirurģiskai nomaiņai, gan TAVI) tiek izvērtētas un noteiktas individuāli katram pacientam vienotā kardiologu, invazīvo kardiologu, anesteziologu un kardioķirurgu konsilijā (“sirds komandas” darbā). Tiek ņemts vērā cilvēka vecums, vispārējais stāvoklis, blakusslimības, mobilitāte, aprūpes iespējas pēc operācijas un citi faktori. Dažkārt nepieciešama arī citu speciālistu konsultācija (internists, pneimonologs, nefrologs, endokrinologs, geriatrs u.c.).
“Sirds komandas” apspriežu laikā katram individuāli pielāgo arī optimālas ārstēšanas stratēģiju (secību, pieejas vietu, laiku, cik ātri procedūra veicama, anestēziju, kā arī, ja nepieciešams, nozīmē papildu izmeklējumus).
Šīs komandas lēmums ir uzskatāms par galveno kritēriju, lai izvēlētos vienu vai otru ārstēšanas metodi. Tikai pacienta vēlmes nav uzskatāmas par indikāciju. TAVI ir mērķtiecīgs, ja paredzamā dzīvildze pārsniedz 1 gadu.
TAVI var veikt tikai centros, kuros ir kardioķirurģijas dienests. Latvijā – tikai Paula Stradiņa klīniskajā universitātes slimnīcā.
Kādos gadījumos priekšroka dodama TAVI?
- Pacientiem, kas pēc “sirds komandas” lēmuma nav piemēroti ķirurģiskai ārstēšanai.
- Vidēja un augsta ķirurģiskā riska pacientiem (ko nosaka pēc speciālām kalkulācijas sistēmām – EuroSCORE I ≥10% un/vai EuroSCORE II/STS score ≥4%).
Nosakot risku pēc European System for Cardiac Operative Risk Evaluation jeb EuroSCORE un Society of Thoracic Surgeons (STS score) kalkulatoriem, tiek ņemti vērā tādi faktori kā vispārējais klīniskais stāvoklis, dzimums (sievietēm risks ir augstāks), vecums un blakusslimības – tādas kā hroniska obstruktīva plaušu slimība, hroniska nieru slimība, ekstrakardiāla arteriopātija, neiroloģiska disfunkcija, nestabila stenokardija, aktīvs endokardīts, anamnēzē miokarda infarkts, iepriekšējas sirds operācijas u.c. No ehokardiogrāfijas datiem tiek vērtēta sirds izsviedes funkcija (<50%) un pulmonālas hipertensijas esamība (sistoliskais plaušu artērijas spiediens >60 mmHg).
- Vecums ≥75 gadiem (sevišķi, ja ir iespējama transfemorālā pieeja).
- Ja ir citi riska faktori, kas nav iekļauti EuroSCORE un STS score riska novērtēšanas sistēmās: porcelāna aorta, anamnēzē staru terapija krūškurvim, hematoloģiskas slimības, spēcīga krūškurvja deformācija vai skolioze, anamnēzē koronāro artēriju šuntēšanas operācija ar funkcionējošiem šuntiem (augsts re-sternotomijas risks).
TAVI ir iespējams veikt arī cilvēkiem ar iepriekš implantētu aortas vai citu sirds vārstuļu bioprotēzi (bioprotēzes deģenerācijas gadījumos).
- Smags pacienta vispārējais stāvoklis, ko nevar izmērīt ne ar STS score, ne EuroSCORE skalu: cilvēks pēdējā gada laikā strauji zaudē svaru, malnutrīcija, muskuļu spēka zudums, nogurums, vājums, aktivitāšu zudums. Šie vispārējie parametri var ietekmēt ķirurģiskas ārstēšanas iznākumu.
TAVI ir kontrindicēta aktīva endokardīta, nepiemērotas anatomijas (piemēram, pārāk liels aortas fibrozais gredzens) un izolētas aortas vārstuļa nepietiekamības gadījumos.
TAVI procedūra
Sākotnēji transkatetrālā aortas vārstuļa implantācija tika veikta, tikai ar cirkšņa artērijas punkciju, kas ierobežoja šīs metodes lietošanu pacientiem ar izteiktu obliterējošu apakšējo ekstremitāšu aterosklerozi. 2006. gadā pasaulē tika sākta arī transapikāla implantācija jeb caur kreisā kambara galotni, kad veic kreisās puses antero-laterālu minitorakotomiju 5.–6. ribstarpā. Šī pieeja tiek izmantota gadījumos, ja transvazāla implantācija nav iespējama.
Jāpiebilst, ka mūsdienās, uzlabojoties tehnoloģijām un samazinoties ievadkatetru diametram, TAVI 90–95% gadījumu veic caur cirkšņa artēriju. Taču to ir iespējams darīt arī caur ascendējošo aortu, zematslēgas vai paduses artēriju, un dažos centros pasaulē to veic arī caur miega artēriju.
Vārstuļu protēzes tiek implantētas, izmantojot palīgierīces – ievadkatetrus, balonus, vadītājstīgas, vadītājkatetrus u.c. Lielo asinsvadu punkciju vietu parasti slēdz ar perkutānām metodēm, izmantojot īpašas slēdzējierīces. Dažkārt izmanto ķirurģisku pieeju artērijai (cut-down).
Transvazālās vārstuļa implantācijas gadījumā ar perkutānu vai dažkārt vaļēju punkciju tiek punktēta cirkšņa artērija, un katetru sistēma tiek ievadīta caur aortu retrogrādā ceļā līdz vārstuļa pozīcijai (sk. 4. att.). Alternatīvi jeb transapikālas implantācijas gadījumā tiek veikta kreisās puses priekšējā sānu minitorakotomija, perikardiotomija un vizualizēta sirds galotne. Caur galotni tiek punktēts sirds kreisais kambaris – antegrādā ceļā katetri tiek aizvadīti līdz aortas vārstulim.
Pēc TAVI parasti nav nepieciešama īpaša rehabilitācijas programma, un pacientus vairākumā gadījumu no stacionāra izraksta 3.–4. dienā.
Specifiskās medicīniskās ierīces
Šobrīd pasaulē pieejams liels skaits vārstuļu, ko var izmantot TAVI procedūrai. Tomēr visas TAVI protēzes iedalāmas divās kategorijās – atkarībā no implantācijas tehnikas:
- Balloon expandable – ar balonu ekspandējamas jeb implantējamas (izgatavotas no tērauda vai citu metālu sakausējumiem);
- Self-expandable – pašekspandējamās jeb pašizpletošās protēzes (izgatavotas no nitinola).
Katram vārstulim ir savas īpatnības (karkasa un lapiņu materiāls, lielums, radiālais spēks, ievadslūžu un ievades sistēmas izmēri, pieļaujamais ārstējamās vārstuļa gredzena izmērs, kā arī vārstuļa pozīcija pēc implantācijas – anulāra vai supraanulāra). Līdz ar to nedaudz atšķirīgi arī sekmīguma kritēriji pēc procedūras, piemēram, aortālās regurgitācijas pakāpe, paravalvulāra šunta iespējamība, nepieciešamība implantēt pastāvīgu stimulatoru.
TAVI operācijas veic ļoti augsta riska pacientiem, kam nav alternatīvas ārstēšanas iespēju. Šiem cilvēkiem ir ļoti dažādas gan anatomiskās, gan strukturālās, gan topogrāfiskās īpatnības. Piemēram:
- kalcinozes pakāpe un lokalizācija (viras, gredzens, izejas trakts);
- aortas vārstuļa gredzena izmērs un dimensijas (cirkulārs, ovāls, asimetrisks);
- ascendējošās aortas izmērs un lokalizācija (dilatēta, horizontāla);
- šaurs koronārais sinuss, divviru vārstulis;
- situācijas, kad TAVI jāimplantē jau iepriekš implantētā protēzē (valve-in-valve operācija);
- neliela kalcinoze un prevalējoša aortālā regurgitācija.
Šī ir tikai daļa no aspektiem, kas jāņem vērā, izvēloties katram pacientam atbilstošu vārstuli.
Vārstulis sastāv no 3 liellopa perikarda lapiņām (vārstuļa virām) un no balonekspandējamā stenta, kas veidots no kobalta–hroma sakausējuma. Tā lielums: 20–29 mm – katram pacientam individuāli.
Vārstulis sastāv no 3 cūkas perikarda lapiņām (vārstuļa virām) un no pašekspandējošā stenta, kas veidots no nitinola. Protēzes augšējā daļā redzami 3 stabilizācijas loki.
Galvenie klīniskie pētījumi
Klīniskajos pētījumos pierādīta TAVI efektivitāte inoperablu un augsta operācijas riska pacientu grupā salīdzinājumā ar ķirurģisku ārstēšanu. Šī metode uzrāda augstu efektivitāti un drošību, kā arī samazina mirstību un uzlabo dzīves kvalitāti.
Sākoties TAVI klīnisko pētījumu programmām Medtronic Corevalve, pašekspandējošās bioprotēzes drošības un efektivitātes dati iegūti prospektīvā multicentru pētījumā augsta ķirurģiska riska pacientiem, un tie uzrāda zemu mirstību sākotnējā periodā un ilgtermiņā bioprotēzes četru gadu rezultātu griezumā.
PARTNER pētījumā tika iekļauti 699 augsta riska pacienti ar smagu slimības formu un randomizēti TAVI procedūrai ar Edwards Sapien bioprotēzi vai ķirurģiskai vārstuļa protezēšanai. TAVI grupā rezultāti uzrādīja zemāku 30 dienu un 1 gada mirstību nekā ķirurģijas grupā. TAVI grupā bija augstāks insulta, bet ķirurģijas grupā augstāks nozīmīgas asiņošanas biežums. Kopumā TAVI tika pierādīta kā ne mazāk efektīva (non-inferior) ārstēšanas metode augsta riska pacientiem un kā pārāka (superior) terapija inoperablo pacientu grupā.
Pēc PARTNER pētījuma tika izveidots nerandomizēts reģistrs (PARTNER Nonrandomized Continued Access registry jeb NCAR) ar 1023 pacientiem, kam veikta TAVI ar Edwards Sapien bioprotēzi. Pētot rezultātus, reģistra dati uzrādīja metodes uzlabošanos – zemākus mirstības un komplikāciju rādītājus operācijas laikā un ilgtermiņā.
PARTNER 2 pētījums bija līdzīgs PARTNER pētījumam, tikai šoreiz lai veiktu randomizāciju starp TAVI un ķirurģisku protezēšanu, tika iekļauti 2032 vidēja riska pacienti. Rezultāti uzrādīja līdzīgus mirstības un insulta rādītājus abās grupās.
Pēdējos gados izveidotas jaunas TAVI ierīces un uzlabotas iepriekšējās paaudzes bioprotēzes, kas nodrošina vairāk sekmīgu procedūru un uzlabo cilvēku dzīvildzi.
Edwards Sapien balonekspandējamās bioprotēzes drošība un efektivitāte pierādīta iepriekš minētajos PARTNER, PARTNER NCAR un PARTNER 2 pētījumos. Turpinot attīstīt medicīnisko tehnoloģiju, izveidota Edwards Sapien 3 bioprotēze, kas nodrošina zemu 30 dienu mirstību, kā arī zemākus smaga insulta un paravalvulāras regurgitācijas rādītājus augsta riska pacientiem/inoperabliem nekā iepriekšējās paaudzes Edwards Sapien bioprotēze.
Nolēgums
Mūsu valstī TAVI ir apstiprināta medicīniska tehnoloģija, un līdz 2021. gada janvārim kopumā Latvijas Kardioloģijas centrā tā veikta 544 reizes. Salīdzinot rezultātus dažādās datubāzēs ar Latvijas datiem, Kardioloģijas centrā novērojams augstāks sekmīgo procedūru rezultāts un zemāka 30 dienu un 1 gada mirstība.
Jāuzsver, ka kritiska aortas vārstuļa stenoze ir uzskatāma par akūtu diagnozi, un palīdzība pacientiem saskaņā arī ar Eiropas un ASV Kardiologu asociācijas vadlīnijām jāsniedz nekavējoties. Tas nozīmē, ka noteiktai pacientu grupai ir iespējams vārstuli nomainīt, lai glābtu dzīvību un pievienotu mūžam kvalitatīvi nodzīvotus gadus.
Jāuzsver, ka TAVI pasaulē izmanto arvien biežāk, to atzīst par efektīvu un drošu. Tā indikācijas un lietojums tiek nepārtraukti paplašināts, iekļaujot arī vidēja riska pacientus. TAVI procedūras izmaksas ir lielas, tomēr ilgtermiņā tas atmaksājas, jo būtiski samazina perioperatīvo morbiditāti, hospitalizācijas biežumu sirds mazspējas dekompensācijas dēļ, samazina 1 un 5 gadu mirstību, tai nav nepieciešama mākslīgā asinsrite, vispārējā intubācijas narkoze. Tāpat, salīdzinot ar ķirurģisko vārstuļa maiņu, ir īsāks hospitalizācijas un intensīvās terapijas palātā pavadītais laiks, tā uzlabo dzīves kvalitāti tūlīt pēc operācijas, un tai nav nepieciešama īpaša rehabilitācija.
Ārkārtīgi augstā mirstības riska dēļ iepriekš minēto datu ignorēšana, proti – laikus neveikta aortas vārstuļa maiņa un neveidota TAVI pacientu rinda, neatbilst mūsdienu medicīnas ētikas principiem. Vienkāršojot teikto – TAVI rindas pacienti mazinvazīvu vārstuļa implantāciju var nesagaidīt.
Foto: Shutterstock
Rakstu lasiet arī „Ārsts.lv” 2021. gada septembra numurā!
Portālā "Ārsts.lv" publicēto rakstu pārpublicēšana iespējama tikai, saskaņojot ar portāla redakciju!