Angelika Krūmiņa: Ērču encefalīts un citas ērču pārnestas slimības
Šī raksta mērķis ir atkārtoti pievērst uzmanību vienai no biežākajām ērču pārnestām infekcijas slimībām Latvijā – ērču encefalītam –, kā arī sniegt nelielu ieskatu par ērlihiozi un arī retākām infekcijas slimībām, kā babezioze un tularēmija. Par vēl vienu ērču pārnestu infekciju – laimboreliozi jeb Laimas slimību – varējāt lasīt žurnāla aprīļa numurā.
Ērču encefalīts
Ērču encefalīts ir viena no aktuālākajām, potenciāli novēršamām centrālās nervu sistēmas infekciju slimībām Eiropā, turklāt nopietna sabiedrības veselības problēma vairāk nekā 27 endēmiskos reģionos Eiropā un Āzijā, tostarp Baltijas valstīs. Eiropas Slimību profilakses un kontroles centra (ECDC) apkopotie 2012.–2016. gada dati liecina, ka ērču encefalīta gadījumu skaitam Eiropā nav tendences pieaugt gadu laikā. Vidēji Eiropā ir 2000–3500 ērču encefalīta gadījumu gadā, Latvijā 2017. gadā reģistrēti 214 ērču encefalīta gadījumi, 2018. gadā – tikai 169, ko var skaidrot ar cilvēku uzvedības pārmaiņām karsto un sauso laikapstākļu dēļ. Saslimstības maksimums Eiropā ir 40–69 gadu vecu cilvēku vidū, ko varētu saistīt ar biežāku atrašanos mežā strādājot, ogojot vai sēņojot.
Vispārīgs slimības raksturojums
Ērču encefalīts (ĒE) ir centrālo nervu sistēmu skaroša infekcijas slimība, ko ierosina vienpavediena ribonukleīnskābi (RNS) saturošs Flaviviridae dzimtas vīruss, ar ko Eiropas un Āzijas valstīs visbiežāk inficējas no Ixodes ģints ērcēm, retāk saslimst, lietojot uzturā nepasterizētu inficētu (kontaminētu) govs, kazas vai aitas pienu. Ērču encefalīta vīrusam izšķir trīs apakštipus – Eiropas (pie mums biežākais), Tālo Austrumu un Sibīrijas –, kuri visi ir sastopami Baltijas valstu reģionā.
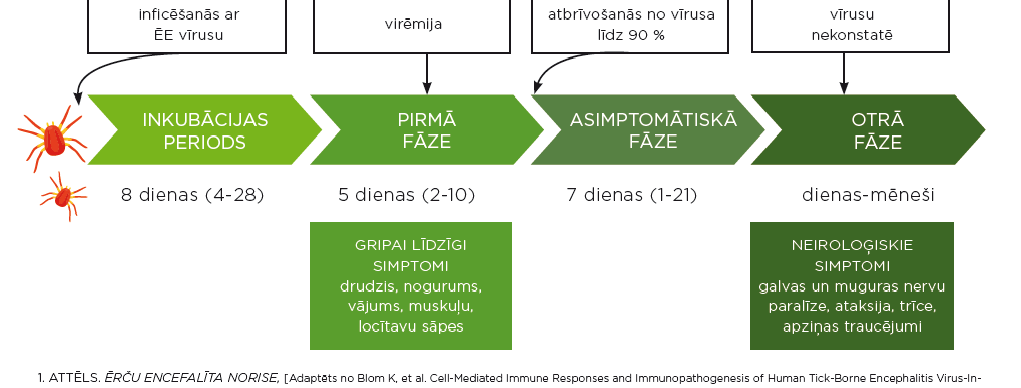
Pēc inficētas ērces koduma tikai 10–30% uzņēmīgu cilvēku attīstās simptomātiska ērču encefalīta infekcija. Ērču encefalītam raksturīga slimības norise divu viļņu veidā (1. attēls). Pēc aptuveni 7–14 dienu inkubācijas perioda (ja inficēšanās notikusi ar inficētu pienu – tikai 3–4 dienas) 90% pacientu attīstās 2–7 dienu gripai līdzīgi simptomi, t.i., drudzis, nespēks, muskuļu un locītavu sāpes (mialģijas un artralģija). To sauc par abortīvo jeb drudža ērču encefalīta formu, un simptomi nereti pāriet paši. Ja pacients spontāni neizveseļojas, seko aptuveni nedēļu ilgs bezsimptomu periods, pēc kura sākas slimības otrā fāze, kad attīstās neiroloģiska simptomātika, kas var izpausties kā:
- meningīts (50%) – raksturīgi klasiskie meningeālie simptomi: sprandas stīvums, pozitīvi Kērniga un Brudzinska simptomi (guļot uz muguras, saliec kāju gūžas locītavā un celī 90 grādu leņķī, mēģina iztaisnot kāju ceļa locītavā, bet nevar, mēģinot iztaisnot saliektā ceļa locītavu, otra kāja arī saliecas ceļa locītavā, Brudzinska simptoms – liecot galvu klāt pie krūtīm, kājas liecas līdzi ceļa locītavā) un fotofobija;
- encefalīts;
- meningoencefalīts (40%) – papildus meningeāliem simptomiem attīstās neiroloģiski simptomi: apziņas un augstāko kognitīvo funkciju traucējumi, mēles muskuļu kontrakcijas, ekstremitāšu trīce, reti – epileptiskas lēkmes;
- meningoencefalomielīts (10%) – papildus iepriekšminētajam attīstās šļauganā parēze (muskuļu vājums) vai paralīze, biežāk skartas rokas, pleci, var skart arī elpošanas muskuļus;
- meningoencefaloradikulīts – papildus meningeāliem un neiroloģiskiem simptomiem raksturīgas muguras smadzeņu saknīšu bojājuma pazīmes (tirpšanas sajūta un jušanas traucējumi ekstremitātēs).
Mirstība no ērču encefalīta sasniedz 1–2% Eiropas, 6–8% Sibīrijas un 20–40% Tālo Austrumu apakštipa gadījumos. Īpašā riska grupā ietilpst vecāka gadagājuma un pacienti ar novājinātu imunitāti.
Līdz 46% izdzīvojušo pacientu attīstās paliekošas ērču encefalīta sekas jeb postencefalītisks sindroms, kas izpaužas ar spinālo nervu parēzēm, dzirdes traucējumiem, dizartriju, mentālo funkciju traucējumiem vai citām pazīmēm.
Diagnostika
Ļoti svarīga diagnostikā ir precīza informācija par ērces kodumu, brīvā laika aktivitātēm (pārgājieni, medības), atrašanos endēmiskajos reģionos, nepasterizēta piena lietošana uzturā, kā arī tas, vai ir veikta vakcinācija pret ērču encefalītu.
Ērču encefalīta pierādīšanai slimības otrajā fāzē nosaka specifiskās antivielas (IgM un IgG) serumā un cerebrospinālajā šķidrumā (CSŠ). IgG antivielas organismā saglabājas visu mūžu, IgM var saglabāties līdz gadam. Specifiskās antivielas cerebrospinālajā šķidrumā var noteikt dažas dienas vēlāk nekā serumā. Jāņem vērā, ka atsevišķos gadījumos IgM antivielas var parādīties arī pēc nesenas vakcinācijas pret ērču encefalītu, tāpēc ir jāzina, kad bijusi pēdējā vakcīnas deva.
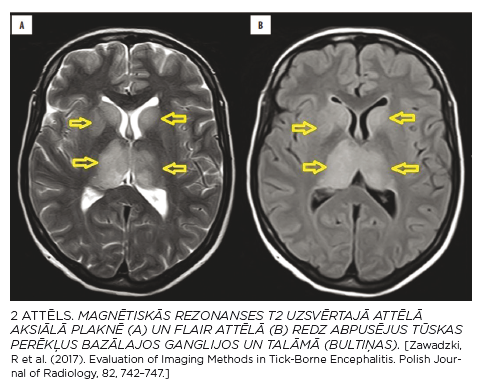
CNS bojājumu vizualizācijai izmanto attēldiagnostikas metodes – datortomogrāfiju un magnētisko rezonansi, kur konstatē bojājumus talāmā, bazālo gangliju, smadzenīšu un muguras smadzeņu priekšējo ragu struktūrās (2. attēls).
Ārstēšana
Specifiskas pretvīrusu terapijas ērču encefalītu gadījumā nav, tāpēc izmanto simptomātisku ārstēšanu: pretdrudža, pretsāpju, pretvemšanas, pretkonvulsiju līdzekļus. Ir svarīgi nodrošināt adekvātu ūdens un elektrolītu līdzsvaru.
Viena no potenciālām ērču encefalīta akūtām komplikācijām ir smadzeņu tūska, t.i., paaugstināts intrakraniālais spiediens, kura terapijā smagos gadījumos var izmantot mannītu vai deksametazonu (pierādījumu līmenis šiem līdzekļiem ir zems).
Pēdējos gados aktīvi diskutē par savulaik aizmirsto ērču encefalīta intravenozu imūnglobulīnu (ĒE IVIG) izmantošanu gan kā profilakses (pēc ērces piesūkšanās), gan kā sākotnējās ārstēšanas izvēles līdzekli pacientiem, kam paredzama smaga slimības norise, – vecāka gadagājuma pacientiem vai pacientiem ar pazeminātu imunitāti. Šobrīd Eiropā nav apstiprināts neviens šāds imūnglobulīnu preparāts, ņemot vērā bažas par iespējamu antivielu atkarīgu ērču encefalīta infekcijas.
Profilakse
Tā kā ērču encefalīta ārstēšanai Eiropā specifisku līdzekļu nav, galvenais veids, kā sevi pasargāt, ir specifisko un nespecifisko profilakses pasākumu veikšana. Svarīgākais ir mazināt ērces piesūkšanās risku, dodoties dabā. Jāizvēlas atbilstošs apģērbs: bikšu galus, ja iespējams, sabāzt zeķēs, nēsāt cieši piegulošas jostas, piedurknes u.tml. Apģērbu ieteicams izvēlēties no slidena un gaiša materiāla, lai ērcēm būtu grūtāk pieķerties un tās būtu labāk pamanāmas, bet apavus – slēgtus, vislabāk zābakus. Ik pa brīdim jāpaskatās, vai nav pieķērusies kāda ērce. Pēc atgriešanās mājās jāveic visa ķermeņa apskate. Ērces, kas atrodas attīstības fāzē (nimfas), var izskatīties kā mazi melni punktiņi. Veikalos ir nopērkami arī dažādi dietiltoluamīdu (DEET) vai permetrīnu saturoši kukaiņu un ērču repelenti, kurus vēlams izsmidzināt uz apģērba un apaviem potīšu līmenī pirms došanās dabā.
No specifiskās profilakses bērniem no viena gada vecuma un pieaugušajiem ir pieejamas divu veidu inaktivētās vakcīnas, ko iesaka visiem, kas dzīvo vai uzturas endēmiskā teritorijā, t.i., ja tur konstatētais ērču encefalīta gadījumu skaits ir vairāk nekā pieci gadījumi uz 100 000 iedzīvotāju. Vakcinācija jums palīdzēs pasargāt sevi no iespējami smagas un letālas infekcijas slimības. Jāatceras, ka pēc pilna vakcinācijas kursa pēc trim gadiem jāveic atkārtota vakcinācija, nākamā revakcinācija parasti jāveic jau pēc pieciem gadiem (gados vecākiem cilvēkiem ik pēc trim gadiem).
Gadījumos, ja kādā imunizācijas posmā nokavēts nākamās devas laiks, imunizācijas plāns nav jāsāk no jauna, jo pētījumos pierādīts, ka jau pēc divu vakcīnas devu ievades saglabājas pietiekama imūnās sistēmas atbilde uz atkārtoto devu ievadi. Šādos gadījumos pacientam ievada nepieciešamo ērču encefalīta vakcīnas devu un nākamo plāno atbilstoši vakcīnas ražotāja ieteikumiem.
Ērlihioze un anaplazmoze
Ērces pārnēsā arī ērlihiozes un anaplazmozes izraisītājus – ērlihijas un anaplazmas, kas ir vienas dzimtas, bet dažādu ģinšu pārstāves, attiecīgi arī slimības izpausmes ir līdzīgas, lai gan ērlihijas primāri inficē monocītus un makrofāgus, anaplazmas – neitrofilos leikocītus. Latvijā 2016. gadā apstiprināti 50 ērlihiozes gadījumu, 2017. gadā – 26, 2018. gadā – 27 gadījumi.
Visbiežāk slimība noris asimptomātiski vai 1–2 nedēļas pēc ērces piesūkšanās attīstās gripai līdzīgi simptomi: drudzis, galvassāpes, nogurums un muskuļu sāpes. Desmitajai daļai anaplazmozes pacientu var būt arī izsitumi, ērlihiozes gadījumā izsitumus novēro ~30%. Retos gadījumos ērlihijas un anaplazmas var ierosināt smagas slimības formas ar sepsi, diseminētu intravaskulāru koagulopātiju, meningoencefalītu u.tml.
Pilnajā asinsainā raksturīga trombocitopēnija, leikopēnija, var būt paaugstināts aknu enzīmu līmenis. Diagnostikā izmanto arī polimerāzes ķēdes reakciju, taču tās jutība ātri mazinās, sākot antibakteriālo terapiju. Antivielu titrs sāk paaugstināties 7–10 dienas pēc inficēšanās, tomēr diagnozes apstiprināšanai nepieciešama atkārtota antivielu titru noteikšana pēc 1–2 nedēļām, kad jābūt vismaz četrkārtējam antivielu pieaugumam.
Pēc Amerikas Infekcijas slimību asociācijas (IDSA) rekomendācijām, pacientam, ja ir aizdomas par ērlihiozi vai anaplazmozi, 10 dienas jāsaņem doksiciklīna terapija. Grūtniecēm vai pacientiem ar doksiciklīna nepanesību var izmantot 10 dienu rifampicīna kursu. Uzlabošanās parasti vērojama jau 24–48 stundu laikā.
Efektīvu vakcīnu šobrīd nav, tāpēc galvenais profilakses princips ir neļaut ērcei sev iekost.
Babezioze
Eiropā Ixodes ricinus ērču pārnestās infekcijas – babeziozes – gadījumu skaits, salīdzinot ar citām ērču pārnestām slimībām, ir neliels – līdz 2013. gadam reģistrēti aptuveni 50 gadījumi, lielākoties Britu salās un Francijā, tomēr vērojama tendence slimībai izplatīties uz Centrāleiropu. Latvijā cilvēku babeziozes gadījumi līdz šim nav konstatēti.
Slimību ierosina Babesia ģints vienšūņu parazīti, kas iznīcina eritrocītus. Parasti slimība norit bez simptomiem. Inkubācijas periods vidēji ilgst 1–3 nedēļas. Pacienti dažkārt sūdzas par gripai līdzīgiem simptomiem, retāk iespējama arī dzelte. Smagākos gadījumos strauji attīstās drudzis – līdz pat 40 °C, smaga anēmija, elpas trūkums, vēlāk var pievienoties dzelte, centrālās nervu sistēmas bojājums, akūta sirds mazspēja un akūti elpošanas traucējumi.
Par babeziozi jādomā tad, ja ir iekodusi ērce, sākušies gripai līdzīgi simptomi, bet stāvoklis neuzlabojas arī pēc terapijas ar doksiciklīnu, jo babēzijas nav jutīgas pret to.
Pilnajā asinsainā un seruma bioķīmijā parasti ir trombocitopēnija un hemolītiskās anēmijas pazīmes (anēmija, hiperbilirubinēmija uz netiešās frakcijas rēķina, paaugstinātas aknu transamināzes). Eiropā diagnoze tiek balstīta uz plānās asins iztriepes mikroskopiju, kur eritrocītos klasiski redzamas apaļas vai ovālas formas babēzijas, un asins parauga polimerāzes ķēdes reakciju.
Simptomātiskiem pacientiem terapijā izmanto azitromicīna un atovakvona kombināciju, smagos gadījumos – klindamicīnu ar hinīnu.
Arī šai slimībai specifiskas profilakses nav, svarīgākais ir izvairīties no ērces piesūkšanās. Jāpievērš uzmanība eritrocītu masu transfūzijām no nepārbaudītiem donoriem.
Tularēmija
Pēdējos gados tularēmijas gadījumu skaits nedaudz pieaug, 2012.–2016. gadā bijuši 300–1100 gadījumu gadā, visvairāk Somijā un Zviedrijā. Latvijā lielākais pēdējos gados reģistrētais tularēmijas gadījumu skaits bijis 2012. gadā, kad sešiem bērniem pēc peldes ūdensžurku apdzīvotā dīķī bija drudzis un limfadenīts. Kopš tā laika Latvijā reģistrēts tikai viens slimības gadījums – 2016. gadā.
Tularēmijas ierosinātājs ir baktērija Francisella tularensis. Cilvēki var inficēties pēc ērču un odu kodumiem, saskaroties ar inficētiem grauzējiem vai to piesārņotām vidēm, lietojot uzturā inficētu pārtiku un pat ieelpojot baktērijas no salmiem un siena. Eiropā galvenās ar tularēmiju inficētās ērču sugas ir Ixodes ricinus un Dermacentor reticulatus, tomēr tikai 1–3% ērču ir inficētas.
Tularēmija ir ļoti lipīga slimība, tāpēc riskam inficēties pakļauts ikviens cilvēks. Pēc aptuveni 3–5 dienu inkubācijas perioda strauji attīstās gripai līdzīgi simptomi: drudzis, drebuļi, galvassāpes un sāpēs muskuļos un locītavās, nelabums, vemšana un caureja. Atkarībā no baktēriju iekļūšanas ceļa cilvēka organismā izšķir sešas galvenās slimības formas:
- ulceroglandulārā – bieži hroniska, strutojoša ādas čūla vietā, kur iekļuvis tularēmijas ierosinātājs, un attiecīgo ādas apvidu drenējošo limfmezglu iekaisums;
- glandulārā – izolēts limfmezglu iekaisums;
- orofaringeālā – hronisks faringīts un kakla limfmezglu iekaisums pēc patogēna norīšanas, retāk attīstās mutes gļotādas čūlas;
- okuloglandulārā – konjunktivīts un lokāla limfadenopātija;
- pneimoniskā – visnopietnākā tularēmijas forma, kas rodas pēc baktēriju ieelpošanas vai hematogēnas izplatīšanās no citiem perēkļiem; raksturīga pneimonijas aina ar letalitāti līdz 30%;
- tifoīdā – atgādina salmonellu sepsi (akūta un smaga gaita – izteikts drudzis, mialģijas, galvassāpes, uzvedības un apziņas traucējumi).
Tularēmijas baktērija ir izturīga, bieži sastopama un viegli izplatāma ārējā vidē, tāpēc klasificēta kā A kategorijas bioterorismā izmantojama viela.
Diagnostika
Par slimību jāaizdomājas, ja ir gripai līdzīgi simptomi ar lokālu limfmezglu iekaisumu. Diagnozes apstiprināšanai veic bioloģisko paraugu (asinis, ādas bojājuma, konjunktīvas vai orofaringeālās iztriepes u.c.) izmeklēšanu.
Terapija un profilakse
Terapijā izmantojami fluorhinolonu, tetraciklīnu vai aminoglikozīdu grupas preparāti.
Efektīvas vakcīnas šobrīd nav, svarīgi ir izvairīties no kontakta ar inficētiem dzīvniekiem un ērcēm. Cilvēkiem pēc saskares ar aizdomīgu vai zināmu tularēmijas inficētu dzīvnieku vai pārtiku ieteicama antibakteriāla profilakse ar ciprofloksacīnu.
Atsauces
Ērču encefalīts
- Beauté Julien, Spiteri Gianfranco, Warns-Petit Eva, Zeller Hervé. Tick-borne encephalitis in Europe, 2012 to 2016. Euro Surveill. 2018;23(45).
- Blom K, Cuapio A, Sandberg JT, et al. Cell-Mediated Immune Responses and Immunopathogenesis of Human Tick-Borne Encephalitis Virus-Infection. Front Immunol. 2018;9:2174.
- Bogovic P, Lotric-Furlan S, Strle F. What tick-borne encephalitis may look like: clinical signs and symptoms. Travel Med Infect Dis. 2010;8:246–250.
- Bogovic P, Strle F. Tick-borne encephalitis: A review of epidemiology, clinical characteristics, and management, World J Clin Cases, 2015; 3(5): 430–441.
- Dumpis U, Crook D, Oksi J. Tick-borne encephalitis. Clin Infect Dis. 1999;28:882–890.
- Elsterova, J., Palus, M., Sirmarova, J., Kopecky, J., Niller, H. H., & Ruzek, D. (2017). Tick-borne encephalitis virus neutralization by high dose intravenous immunoglobulin. Ticks and Tick-Borne Diseases, 8(2), 253–258.
- Fedorowicz Z, Ehrlich A. Tick borne encephalitis: Overview and Recommendations, Nov 2016; https://www.dynamed.com/topics/dmp~AN~T900314/Tickborne-encephalitis#General-Information.
- Golovljova I, Vene S, Sjölander KB, Vasilenko V, Plyusnin A, Lundkvist A. Characterization of tick-borne encephalitis virus from Estonia. J Med Virol. 2004;74(4):580-8.
- Holzmann H. Diagnosis of tick-borne encephalitis. Vaccine. 2003;21 Suppl 1:S36–S40.
- Horger M, Beck R, et al. Imaging findings in tick-borne encephalitis with differential diagnostic considerations. 2012; 199(2): 420–427.
- https://www.spkc.gov.lv/upload/Infekcijas_lim_statistika/Citi_epid_bileteni/copy_of_11_18.pdf
- Jääskeläinen AE, Sironen T, Murueva GB, Subbotina N, Alekseev AN, Castrén J, et al. Tick-borne encephalitis virus in ticks in Finland, Russian Karelia and Buryatia. J Gen Virol. 2010;91(11):2706-12.
- Kaiser R. Tick-borne encephalitis. Infect Dis Clin North Am. 2008;22:561–575.
- Kollaritsch H, Krasilnikov V, Holzmann H, Karganova G, Barrett A, Süss J, et al. Background document on vaccines and vaccination against tick–borne encephalitis. Geneva, WHO Strategic Advisory Group of Experts on Immunization. Pieejams: http://www.who.int/immunization/sage/6_TBE_backgr_18_Mar_net_apr_2011.pdf
- Lindquist L, Vapalahti O. Tick-borne encephalitis. Lancet. 2008;371(9627):1861-71.
- Mansfield KL, Johnson N, Phipps LP, Stephenson JR, Fooks AR, Solomon T. Tick-borne encephalitis virus - a review of an emerging zoonosis. J Gen Virol. 2009;90(8):1781-94.
- Misić Majerus L, Daković Rode O, Ruzić Sabljić E. [Post-encephalitic syndrome in patients with tick-borne encephalitis] Acta Med Croatica. 2009;63:269–278.
- Penevskaia N.A., Rudakov N.V., 2010. Efficiency of use of immunoglobulin preparations for the postexposure prevention of tick borne encephalitis in Russia (a review of semicentennial experience). Med Parazitol. (Mosk), 53–59.
- Randolph SE, Asokliene L, Avsic-Zupanc T, Bormane A, Burri C, Gern L, et al. Variable spikes in tick-borne encephalitis incidence in 2006 independent of variable tick abundance but related to weather. Parasit Vectors. 2008;1(1):44.
- Saksida A, Duh D, Lotric-Furlan S, Strle F, Petrovec M, Avsic-Zupanc T. The importance of tick-borne encephalitis virus RNA detection for early differential diagnosis of tick-borne encephalitis. J Clin Virol. 2005;33:331–335.
- Schöndorf I, Schönfeld C, Nicolay U, Zent O, Banzhoff A. Response to tick-borne encephalitis (TBE) booster vaccination after prolonged time intervals to primary immunization with the rapid schedule. Int J Med Microbiol. 2006;296 Suppl 40:208–212.
- Stanek G, Wormser GP, Gray J, Strle F. Lyme borreliosis. Lancet. 2012;379:461–473.
- World Health Organization (WHO) Vaccines against tick-borne encephalitis: WHO position paper. Wkly Epidemiol Rec. 2011;86:241–56.
- Zavadska D, Anca I, et al. Recommendations for tick-borne encephalitis vaccination from the Central European Vaccination Awareness Group (CEVAG). Human Vaccines & Immunotherapeutics, 2013; 362–374.
- Zawadzki, R., Garkowski, A., Kubas, B., Zajkowska, J., Hładuński, M., Jurgilewicz, D., & Łebkowska, U. (2017). Evaluation of Imaging Methods in Tick-Borne Encephalitis. Polish Journal of Radiology, 82, 742–747.
Ērlihioze un anaplazmoze
- https://www.spkc.gov.lv/upload/Infekcijas%20slim%C4%ABbas/Bileteni/12_17.pdf
- https://www.spkc.gov.lv/upload/Infekcijas_lim_statistika/Citi_epid_bileteni/copy_of_11_18.pdf
- Chapman AS, Bakken JS, Folk SM, et al. Diagnosis and management of tickborne rickettsial diseases: Rocky Mountain spotted fever, ehrlichioses, and anaplasmosis-United States: a practical guide for physicians and other health-care and public health professionals. MMWR Recomm Rep. 2006;55(RR-4):1–27.
- Christova I, Schoul, L, van de Pol I, Park J, Panayotov S et al. High prevalence of granulocytic ehrlichiae and Borrelia burgdorferi sensu lato in Ixodes ricinus ticks from Bulgaria. Journal of clinical microbiology, 2001, 39(11): 4172-4174.
- Egyed L, Élő P, Sréter-Lancz Z, Széll Z, Balogh Z and Sréter T. Seasonal activity and tick-borne pathogen infection rates of Ixodes ricinus ticks in Hungary. Ticks and tick-borne diseases 2012, 3(2), 90-94.
- Stuen, S. Anaplasma phagocytophilum-the most widespread tick-borne infection in animals in Europe. Veterinary research communications 2007, 31(1): 79-84.
- Sanchez, E., Vannier, E., Wormser, G. P., & Hu, L. T. (2016). Diagnosis, Treatment, and Prevention of Lyme Disease, Human Granulocytic Anaplasmosis, and Babesiosis. JAMA, 315(16), 1767.
- https://www.msdmanuals.com/professional/infectious-diseases/rickettsiae-and-related-organisms/ehrlichiosis-and-anaplasmosis
- Bakken JS and Dumler JS. Human Granulocytic Anaplasmosis. Infectious disease clinics of North America, 2015, 29(2): 341-355.
- Ismail, N., Bloch, K. C., McBride, J. W. (2010). Human Ehrlichiosis and Anaplasmosis. Clinics in Laboratory Medicine, 30(1), 261–292. doi:1016/j.cll.2009.10.004
- Sanchez, E., Vannier, E., Wormser, G. P., & Hu, L. T. (2016). Diagnosis, Treatment, and Prevention of Lyme Disease, Human Granulocytic Anaplasmosis, and Babesiosis. JAMA, 315(16), 1767.
Babezioze
- Martinot M, Zadeh MM, Hansmann Y, Grawey I, Christmann D,Aguillon S, Jouglin M, Chauvin A, De Briel D. Babesiosis in immunocompetent patients, Europe. Emerg Infect Dis.2011;17:114–6.
- Vannier E, Krause PJ. Human babesiosis. N Engl J Med.2012;366:2397–407.
- Hunfeld KP, Hildebrandt A, Gray JS. Babesiosis: recent insightsinto an ancient disease. Int J Parasitol. 2008;38:1219–37
- Sanchez, E., Vannier, E., Wormser, G. P., & Hu, L. T. (2016). Diagnosis, Treatment, and Prevention of Lyme Disease, Human Granulocytic Anaplasmosis, and Babesiosis. JAMA, 315(16), 1767.
- Hildebrandt, A., Gray, J. S., & Hunfeld, K.-P. (2013). Human Babesiosis in Europe: what clinicians need to know. Infection, 41(6), 1057–1072.
Tularēmija
- https://ecdc.europa.eu/sites/portal/files/documents/AER_for_2016-tularaemia.pdf
- https://spkc.gov.lv/en/news/arhivs/get/nid/432
- https://www.spkc.gov.lv/upload/Infekcijas%20slim%C4%ABbas/Bileteni/12_17.pdf
- Maurin, M., & Gyuranecz, M. (2016). Tularaemia: clinical aspects in Europe. The Lancet Infectious Diseases, 16(1), 113–124.
- http://www.nmpd.gov.lv/nmpd/katastrofu_medicina/arkartas_situacijas/bistamas_infekcijas_slimibas/tularemija/
- Gyuranecz M, Rigó K, Dán A, et al. Investigation of the ecology of Francisella tularensis during an inter-epizootic period. Vector Borne Zoonotic Dis 2011; 11: 1031–35.
- WHO. WHO guidelines on tularaemia. Geneva: World Health Organization Press, 2007.
Rakstu lasiet arī „Ārsts.lv” 2019. gada maija numurā!
Portālā "Ārsts.lv" publicēto rakstu pārpublicēšana iespējama tikai, saskaņojot ar portāla redakciju!

